24B. Fixace N2
Asimilace N – ze sloučenin anorganických do organických – běžné (rostliny, mikroorganismy obecně)
N2 – inertní, problém převést na sloučeninu
- kyslíkaté – výboje
- redukce na NH3 – energeticky náročná
N2
+ 3H2 ![]() 2NH3 DG°' = 32,6 kJ.mol-1
2NH3 DG°' = 32,6 kJ.mol-1
Technologicky – katalýza (pův. Os a U, dnes Fe3+,
400 – 650 oC, 10 – 40 MPa) – Haber-Bosch 1913
spotřebuje
ca 1% veškeré celosvětově produkované energie
Biochemicky – enzymová katalýza + ATP
25B Nitrogenasa
Probíhá podle rovnice
N2 + 8H+ + 8e- ![]() 2NH3
+ H2
2NH3
+ H2
na každý elektron se spotřebují 2 ATP, tedy
16 ATP ![]() 16
ADP + 16 Pi
16
ADP + 16 Pi
Celkově
N2 + 4NADH+ H+ + 16MgATP ![]() 2NH3
+ H2 + 4NAD+ + 16MgADP + 16Pi
2NH3
+ H2 + 4NAD+ + 16MgADP + 16Pi
Tato redukce je omezena na několik mikroorganismů – symbiotické a volně žijící
Rhizobium – symbiont vikvovitých rostlin
Azotobacter, Klebsiella, Clostridium a cyanobacterie (vodní)
Reakce je katalysována nitrogenázovým komplexem složeným z FeS-proteinu dinitrogenasa reduktasy (složena ze 2 podjednotek o ca 65 kD, obsahuje 4Fe a 4S na dimer, citlivá na kyslík) a MoFe-proteinu dinitrogenasy (a2b2 heterotetramer s velkým redoxním centrem obsahujícím Fe4S3 a Fe3MoS3 spojené 3 sulfidovými skupinami)
Nitrogenasová reakce může být rozložena do 3 kroků:
- redukce FeS-proteinu
externím donorem elektronů
- redukce MoFe-proteinu
redukovaným FeS-proteinem
- redukce N2
MoFe proteinem
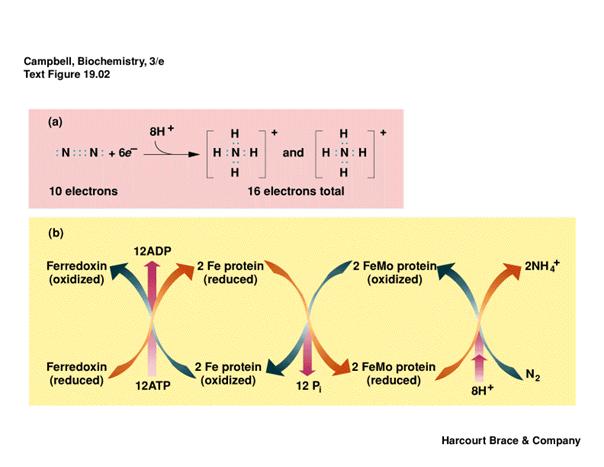
První reakce vyžaduje NADH a je katalysována feredoxinem.
Ve druhém stupni dochází ke spřažení s exergonickým pochodem – hydrolýzou ATP. Podstatou je snížení redoxpotenciálu (z -350 mV na -450 mV) po fosforylaci proteinu, to umožní redukovat koncový enzym – FeMo-protein o nízkém E’0, jenž je pak schopen redukce N2.
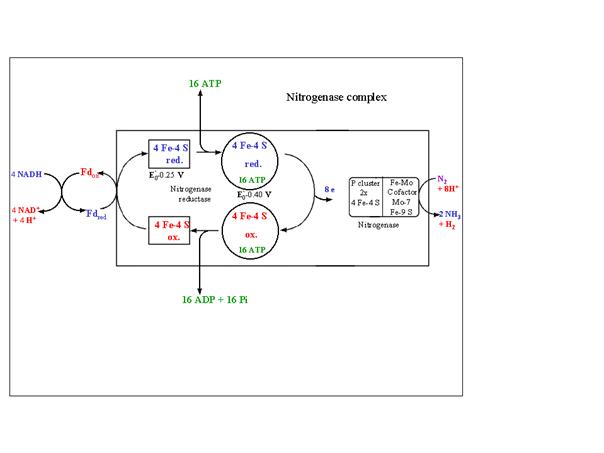
Úloha Fe4S4 při redukci dinitrogenasy
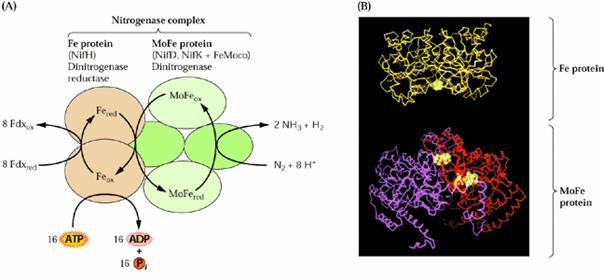
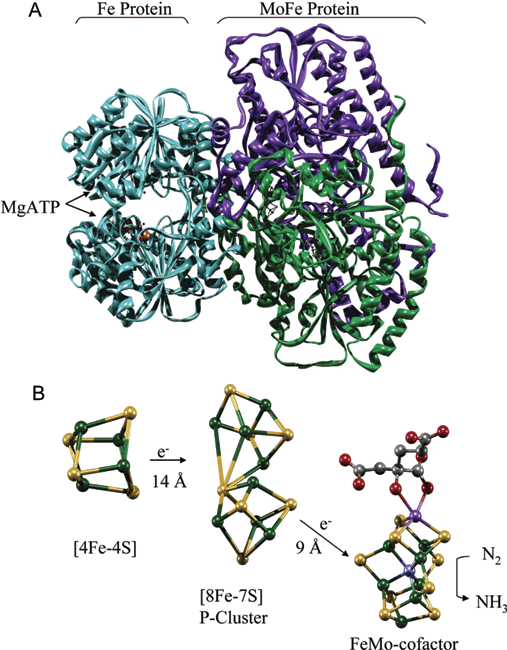
Přenos elektronu mezi klastry
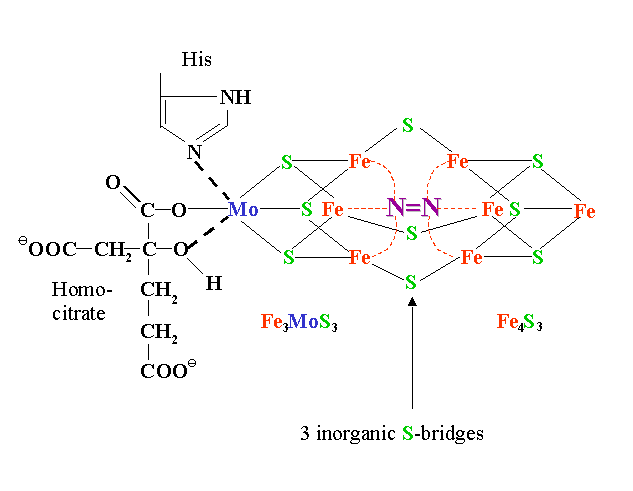
Vazba N2 v klastrech dinitrogenasy
Nitrogenasa (podobně jako RUBISCO) je syntesována ve velkých množstvích, u diazotofytů tvoří až 10% všech bílkovin.
Nitrogenasa redukuje i jiné substráty se strukturou podobnou N2, dobrým měřítkem její aktivity je reukce acetylenu:
HCCH + 2e- + 2H+ ![]() H2CCH2
H2CCH2
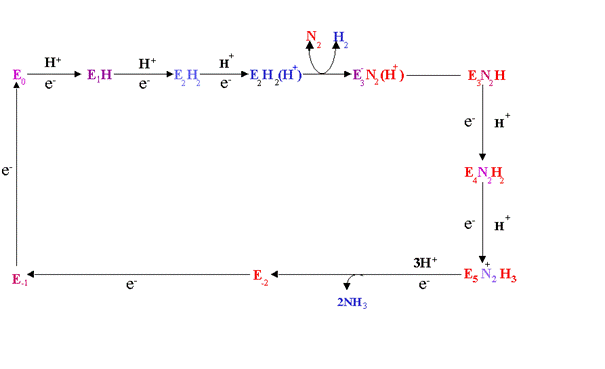
Schema mechanismu
redukce N2
Problém citlivosti ke kyslíku, produkce leghemoglobinu odčerpávajícího O2 (v rostlinné buňce, kodován v jejím jádře.
Symbiosa – rostlina zásobuje symbionta metabolity (z TCA).
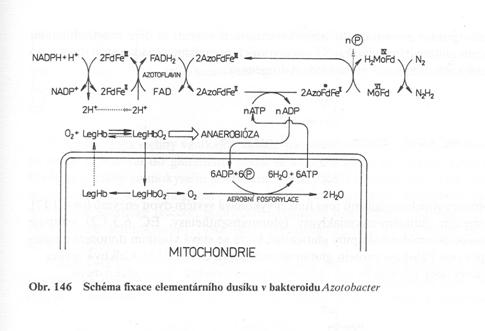
Lokalisace enzymů
redukce dusíku
Možnosti GMO – nitrogenázy v rostlinách.
Jiné typy nitrogenas (V místo Mo, účast azotoflavinu aj.)