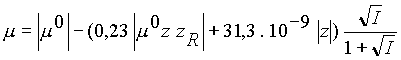
Kapilární izotachoforéza
Elektroforetické metody jsou založeny na pohybu nabitých částic v elektrickém poli. Rychlost částice ( v ) je přímo úměrná intenzitě elektrického pole ( E ) a elektroforetické pohyblivosti (
m ) :v =
m . E
Elektroforetická pohyblivost
- vztažena vždy na prostředí, ve kterém se látka pohybuje
- jednotky m2V-1s-1
- znaménko určuje směr pohybu iontu
pohyblivost kationtů - kladné znaménko
pohyblivost aniontů - záporné znaménko
- hodnota pro většinu iontů ~ 10
-8H+ 362,5 x 10-9 m2V-1s-1
OH- 205,5 x 10-9 m2V-1s-1
Skutečná pohyblivost - vliv vnějšího prostředí
vliv iontové síly - Onsagerova rovnice
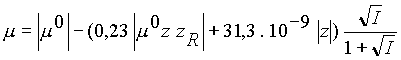
ď
mď - iontová pohyblivostď
moď - limitní iontová pohyblivostď
zRď - náboj protiontuI - iontová síla
vliv teploty
m
(T) = m (To) [ 1 + a (T - To)]a ![]() 0,02
0,02
zvýšením teploty o 10 oC se zvýší pohyblivost přibližně o 20%
Efektivní pohyblivost -
vliv chemických rovnováh na pohyblivost iontůTiselius:
Látka, přítomná v roztoku ve více formách, které jsou navzájem v rychlé dynamické rovnováze, migruje elektrickým polem jako jediná látka o určité efektivní pohyblivosti m :
![]()
xi - molární zlomky jednotlivých forem látky
m
i - iontové pohyblivosti jednotlivých forem látkyPrincip metody
Zónová elektroforéza
Vzorek separovaných látek se pohybuje v prostředí základního elektrolytu, který zaručuje udržení konstantního homogenního elektrického pole. Jednotlivé separované látky se pohybují různou rychlostí podle svých elektroforetických pohyblivostí.
Izotachoforéza
Vzorek je umístěn mezi vedoucí a koncový elektrolyt. Vedoucí elektrolyt má nejvyšší pohyblivost a koncový elektrolyt nejnižší pohyblivost v celém systému. Po nastavení těch
to podmínek jsou jednotlivé separované látky prostředím, které zaručuje udržení konstantního elektrického pole. Jednotlivé separované látky se pohybují stejnou rychlostí a jsou za sebou zařazeny podle svých elektroforetických pohyblivostí.
Koncentrace v izotachoforetických zónách
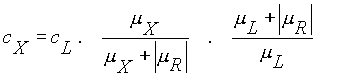
Při analýzách s neměnnou koncentrací vedoucího elektrolytu je koncentrace látek v zónách konstantní
- lze využít délku zóny pro kvantitativní vyhodnocení
koncentrace látek v původním vzorku nemá žádný vliv na výslednou koncentraci látky v adjustované izotachoforetické zóně
Průběh izotachoforetické analýzy dikarboxylových kyselin :
Operační systém
|
Vedoucí ion |
10 mmol/l HCl |
|
Protiion |
b - alanin |
|
pH vedoucího elektrolytu |
4.0 |
|
Koncový elektrolyt |
5 mmol/l kys. propionová |
Zásobník koncového elektrolytu je naplněn roztokem 5 mmol/l kys. propionové a zásobník vodícího elektrolytu s kapilárami naplněn 5 mmol/l HCl upravené
b - alaninem na pH 4.0Pomocí dávkovacího kohoutu je na rozhraní mezi vodící a koncový elektrolyt nanesena směs dělených dikarboxylových kyselin.
K separaci dochází po zapojení zdroje vysokého napětí.